Klf5通过对ICM和TE基因的双重调控,建立了双电位细胞命运
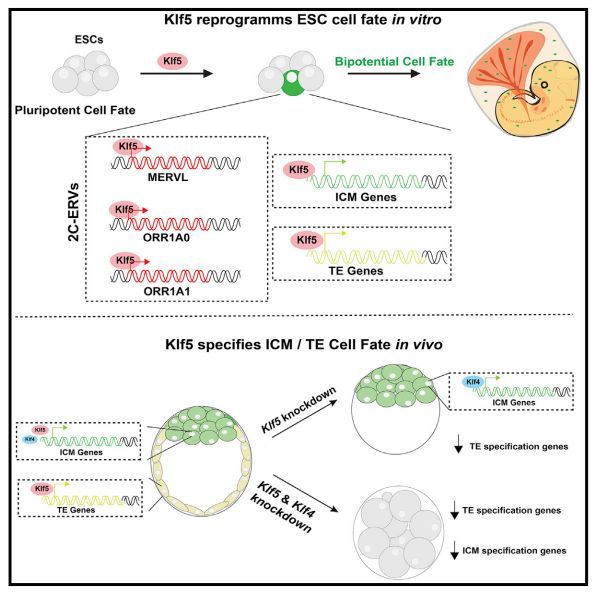
小鼠植入前胚胎的早期卵裂球具有双电位细胞命运,能够在胚泡中产生胚胎和胚胎外系。在这里,作者鉴定了三种主要的两细胞阶段(2C)特异性内源性逆转录病毒(ERVs)作为这种双潜能可塑性的分子标志。利用这三种2c特异性erv的长末端重复序列(ltr),作者发现Kruppel-like factor 5 (Klf5)是它们主要的上游调节因子。

Klf5对双电位细胞命运至关重要; 一个Klf5过表达的胚胎干细胞(ESC)在嵌合胚胎中产生终末分化的胚胎和胚胎外系,Klf5直接诱导内细胞质量(ICM)和滋养胚层(TE)规范基因。有趣的是,Klf5和Klf4在ICM规范中冗余地发挥作用,而仅Klf5缺陷就会损害TE规范。Klf5受到多个2c特异性转录因子的调控,尤其是Dux,并且Dux/Klf5轴是进化保守的。2c特异性转录程序与Klf5汇合,建立双电位细胞命运,使ICM和TE基因双重激活的细胞状态。

图片来源:https://doi.org/10.1016/j.celrep.2021.109982
哺乳动物着床前发育是由母体遗传因素和合子基因组激活过程中转录的合子基因启动的。小鼠受精卵和两细胞阶段(2C)卵裂球是全能的,能够产生可育的成年有机体所需的所有细胞类型。全能性在随后的发育阶段逐渐受到限制,但分裂期卵裂球保留双势细胞命运,产生内细胞团(ICM),主要形成胚胎本身,滋养外胚层(TE),产生胚胎外胎盘组织。
双电位细胞命运的一个显著分子标志是强烈但短暂的内源性逆转录病毒(ERVs)诱导。MERVL转录本是2C - 4C胚珠转录组中表达量最高的转录本之一; 在发育过程中,随着卵裂期卵裂球的发育可塑性变窄,其水平迅速下降。在多能小鼠胚胎干细胞(ESCs)中,产生所有的胚胎细胞类型,但很少产生胚胎外系,在罕见的细胞群中诱导MERVL通常与扩大的细胞命运可塑性相关,使分化向胚胎和胚胎外系。
然而,这样的MERVL+ ESCs并不等同于2C的卵裂粒,既不具有全能的细胞命运潜能,也不具有2C的转录组。相反,在作者的研究中,MERVL+ ESCs,即双潜能ESCs,表现出胚胎和胚外潜能,在中等水平诱导MERVL,并在功能上类似于双潜能胚珠,其发育潜力比2C胚珠更受限。
由于MERVL是2C胚珠的一个分子标志,人们推测直接调控MERVL并在ZGA处短暂峰值的转录因子可以建立一个转录景观,从而实现双电位细胞命运。双homeodomain转录因子Dux就是这样一个候选因子,它在ZGA开始时诱导2C胚珠中直接促进MERVL的表达。合子表达的Dux及其母系遗传的上游调控因子Dppa2、Dppa4、Nelfa和Smarca5被推测在转录层次的顶层发挥作用,这些调控因子控制着ZGA的发生、MERVL的诱导和2c特异性细胞命运潜能的调控。
然而,单独使用Dux、Smarca5或Nelfa,或Dppa2和Dppa4联合使用,均不能损害小鼠ICM或TE的特异性,这表明这些因素对建立/维持双潜能细胞命运并不重要。因此,使用MERVL作为双电位细胞命运的唯一分子标记可能不足以识别双电位细胞发育命运的关键调控因子

lf5通过对ICM和TE基因的双重调控,建立了双电位细胞命运
图片来源:https://doi.org/10.1016/j.celrep.2021.109982
通过使用三种2c特异性erv作为双电位细胞命运的标志,我们发现克虏伯样因子(Klf5)是赋予胚胎和胚胎外系发育潜力的重要调控因子。虽然之前的研究已经描述了Klf5敲除胚胎的着床前缺陷,但Klf5在双电位细胞命运中的功能重要性,以及Klf5与其他Klf转录因子在着床前发育中的功能相互作用在很大程度上仍不清楚。
作者的研究表明,Klf5在一个单一的、多能的ESC中过表达,在嵌合胚胎中赋予双电位细胞命运。小鼠遗传学研究表明,Klf5在促进TE规范方面发挥了重要作用,Klf5和Klf4在赋予ICM细胞命运的效力方面发挥了冗余作用。由于Klf5直接诱导ICM和TE基因,该数据表明,双潜能发育潜能的分子本质是一种共同表达ICM和TE基因的细胞状态。
来源:生物谷

 微信公众号
微信公众号 京公网安备11010502033649
京公网安备11010502033649